在製藥產業中,資料完整性(Data Integrity)是確保產品品質與法規符合的核心基礎。隨著USP <1029>指南草案發布,文件中有提出ALCOA++原則,進一步強化資料可追溯性,確保從資料產生到保存的全生命週期皆具透明性與可信度。
什麼是 ALCOA++?
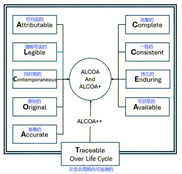
ALCOA++包含可歸屬、清晰可辨、同步記錄、原始性、準確性、完整性、一致性、持久性、可獲取性與可追溯性等十項原則,確保資料在整個生命週期中皆可被追蹤與驗證。

LCOA原則最早由美國FDA於2007年提出,包含可歸因性、易讀性、同步性、原始性和準確性五個核心屬性;隨後,歐盟EMA在2010年擴展爲ALCOA+,強化了完整性、一致性、持久性和可獲取性四項要求;最新提出ALCOA++是將所有這些關鍵概念置於可追溯性的框架之下,強調數據修改需全程留痕,確保操作或變更可追溯。

在數字化轉型浪潮中,能最先採用這一框架的企業,必將贏得市場的長期信任。
可追溯性之鏈強調數據必須能夠追蹤其來源、變更路徑及最終狀態,包含從原輔料檢測到成品放行的全過程。這種設計不僅滿足審核機關要求,更在內部審核中提供無可辯駁的證據鏈。例如:
★對現有條目的任何修改均不應遮蓋原始條目,修改需附說明及日期,並標明修改人。
★記錄本頁面和工作記錄單應連續使用,資訊記錄需按時間順序進行。
★所有日期均應採用清晰明確的格式,標明時、日、月、年。
★應有一份包含每位責任人的簽名或首字母的正式記錄,或包含在文件中。
★所有用於數據收集和評估的GMP記錄均應經過適當的第二人審覈(包括日期和簽名)以驗證其符合適用程序及記錄條目的完整性和準確性。
總之,從最早的“記下來”,到後來的“準數據”,再到今天的“可追溯”, ALCOA++原則通過十個維度的緊密交織,構建了一個從數據產生到最終檔案的完整追溯鏈條,爲製藥、醫療、臨牀測試等受監管行業提供了堅實的數據完整性保障。





